HPV vaccinaties en baarmoederhalskanker?
Allereerst de feiten, kort samengevat
Baarmoederhalskanker is een zeldzame ziekte.
Het doel van de vaccinatie is om de sterfte aan baarmoederhalskanker in Nederland te halveren: van tweehonderd naar honderd per jaar.
Er zijn jaarlijks rond de 600 nieuwe diagnoses van baarmoederhalskanker en dat aantal daalt. Dat komt omdat we in Nederland een goed bevolkingsonderzoek hebben. Hierdoor worden heel veel gevallen al ontdekt in een voorstadium, waarin het nog geen kanker is.
HPV staat voor humaan papiloma virus.
Er zijn heel veel verschillende types van het virus.
Je kunt het HPV oplopen na seksueel contact. Daarbij is huid op huid-contact al voldoende. Dat betekent niet dat het virus er voor zorgt dat je daadwerkelijke baarmoederhalskanker krijgt.
Maar liefst 80% van de vrouwen krijgt ooit in haar leven een HPV-infectie en in bijna alle gevallen geneest deze vanzelf.
Het virus op zich veroorzaakt niet direct baarmoederhalskanker doch een langdurige infectie met dit virus veroorzaakt voorstadia van baarmoederhalskanker en uiteindelijk krijgt 2% van de vrouwen, met zo'n langdurige infectie, baarmoederhalskanker. Daarom is het meedoen aan het bevolkingsonderzoek naar baarmoederhalskanker zo belangrijk.
De virus types HPV 16 en HPV 18 zijn verantwoordelijk voor 70% van de gevallen van baarmoederhalskanker.
Het vaccin waarmee wordt ingeënt, beschermt volgens onderzoek tegen deze 2 types van HPV-infecties.
De belangrijkste voorwaarden voor de werking is dat op het moment van inenting niet al een infectie met een van deze twee virussen is, want dan doet het vaccin weinig of niets. (Uit, gelukkig maar 1 studie, zou moeten blijken dat vaccinatie dan zelfs een verhoging van de kans op baarmoederhalskanker zou kunnen geven)
Over de werking van de vaccins bij meisjes jonger dan 15 jaar is nauwelijks iets wetenschappelijks bekend.
Over de werking van de vaccins op langere termijn en of die inderdaad baarmoederhalskanker kunnen voorkomen, alsmede over de bijwerkingen is wetenschappelijk niets bekend.
'Prik en bescherm!', is de slogan van de GGD-campagne die meisjes oproept zich te laten inenten tegen baarmoederhalskanker. Sommige GGD's lokken zelfs meisjes met iPod's.
Geen wonder dat bezorgde artsen en wetenschappers waarschuwen dat er aan vaccinatie ook risico's verbonden zijn.
Het is aan ieder meisje en haar ouders zelf om te beoordelen of men wil deelnemen aan deze vaccinatie doch gelet op alle informatie lijkt het ons dat heel de HPV campagne de overheid, en dus ons allemaal veel geld kost en vrouwen weinig of geen voordelen en misschien wel (nog) onbekende nadelen biedt.
Het risico is ook niet ondenkbeeldig dat de groep die nu gevaccineerd wordt zich beschermd gaat wanen tegen baarmoederhalskanker en daardoor later in het leven de uitnodigingen voor het bevolkingsonderzoek naar baarmoederhalskanker gaat negeren met mogelijk averechtse gevolgen van dien.
Wellicht had de overheid dat geld beter kunnen steken in onderzoek naar de risicofactoren van baarmoederhalskanker en of HPV-vaccinatie kan worden ingezet bij vrouwen wiens lichaam zelf het virus niet geneest.
Om onduidelijke redenen heeft de overheid ondanks alles redelijk snel beslist om deze vaccinatie op te nemen in het Rijksvaccinatieprogramma, de grote invloed van de farmaceutische industrie zal zeker een van die redenen zijn.
Volgens een Amerikaanse wetenschapper die het onderzoek naar het HPV-vaccin mede gedaan heeft is HPV-vaccinatie op grote schaal een groot experiment met onbekende gevolgen.
Een onderzoek dat bijwerkingen, als gedragsveranderingen, laat zien wordt meteen na publicatie (tijdelijk) verwijderd??
Hier een analyse van de studies over de HPV-vaccinatie. Hieruit blijkt dat slechts in 2 van de 16 studies een echt placebo gebruikt en verder dat de bijwerkingen inderdaad veel meer zijn dan bij andere vaccinaties.
Hier nog een video over de HPV-vaccinatie.
Inmiddels, nu ruim 10 jaar later, januari 2020, laat een studie zien dat de HPV-vaccins eigenlijk helemaal niet werkzaam zijn.
Hieronder twee rapporten van deskundigen,
Onvoldoende gronden voor opname van vaccinatie tegen Humaan papillomavirus in het Rijksvaccinatieprogramma door de epidemiologen Mw.prof.dr.ir.F.E.van Leeuwen, Mw.drs.I.M.C.M.de Kok, hr.prof.dr.J.D.F.Habbema, hr.prof.dr.J.W.W.Coebergh (ook sociaal-geneeskundige) en gynaecologisch oncoloog Mw.prof.dr.M.J.E.Mourits
en HPV-vaccinatie weinig zinvol door drie artsen van het Nederlands Huisartsen Genootschap (NHG).
Onvoldoende gronden voor opname van vaccinatie tegen Humaan papillomavirus in het Rijksvaccinatieprogramma
I.M.C.M. de Kok, J.W.W. Coebergh, J.D.F. Habbema, M.J.E. Mourits en F.E. van Leeuwen
Minister Klink van Volksgezondheid, Welzijn en Sport wil vanaf september 2009 starten met het landelijk vaccinatieprogramma tegen het Humaan papillomavirus (HPV). Dat blijkt uit zijn brief aan de Tweede Kamer van 8 juli jongstleden (www.minvws.nl/kamerstukken/pg/2008/vaccinatie-tegen-baarmoederhalskanker.asp). Hij volgt hiermee het advies van de Gezondheidsraad op om HPV-vaccinatie voor 12-jarige meisjes in het Rijksvaccinatieprogramma op te nemen. Voor meisjes van 13-16 jaar oud wordt door de raad een inhaalprogramma geadviseerd. 1 Onlangs gingen Van Rossum et al. in dit tijdschrift in op de achtergronden van deze vaccinatie. 2
Wij hebben grote bezwaren tegen opname van HPV-vaccinatie in het Rijksvaccinatieprogramma op zo korte termijn. Op basis van de 7 criteria die de Gezondheidsraad hanteert bij zijn advies 1 beargumenteren wij dat aan 5 daarvan onvoldoende wordt voldaan en dat de minister en de Tweede Kamer beter kunnen wachten met het nemen van een dergelijk besluit. De 7 criteria staan in de tabel.
gaat het om een ziekte die ernstig is voor individuen en die een omvangrijke groep treft?
Baarmoederhalskanker is een ernstige ziekte, maar is in Nederland in de laatste decennia, en ook nog in de laatste jaren, steeds zeldzamer geworden. In 2005 werd bij 687 vrouwen de diagnose ‘baarmoederhalskanker’ gesteld en in 2007 stierven 204 vrouwen als gevolg van deze ziekte (bron: Nederlandse Kankerregistratie; www.ikcnet.nl). Dit betrof onder de vrouwelijke populatie 0,3% van de totale sterfte en 1,8% van de sterfte onder de 50 jaar (bron: Centraal Bureau voor de Statistiek; www.cbs.nl).
Nederland is een van de landen met een effectief en efficiënt screeningsprogramma. 3 4 Hierdoor zijn de incidentie en de sterfte in ons land internationaal gezien zeer laag: de op wereldniveau gestandaardiseerde cijfers (‘world standardised rate; WSR) bedragen voor ons land respectievelijk 5,8 en 1,6 per 100.000 vrouwen per jaar (bron: www.ikcnet.nl), terwijl de WSR voor de wereldwijde variatie in incidentie 2-69 per 100.000 bedraagt en in mortaliteit 1-56 per 100.000 (www-dep.iarc.fr; doorklikken op ‘GLOBOCAN 2002’). In Nederland wordt niet door alle vrouwen aan het bevolkingsonderzoek deelgenomen, en veel van de sterfte aan baarmoederhalskanker vindt plaats bij vrouwen die niet of niet volledig zijn gescreend. 5
staat vast dat vaccinatie werkzaam is in het voorkómen van ziekte of het reduceren van symptomen?
Effectiviteit van vaccinatie. De effectiviteit van vaccinatie tegen baarmoederhalskanker is nog niet aangetoond. De Gezondheidsraad is optimistisch, maar heeft nog geen bewijzen. Een aantal trials waarin de beschikbare vaccins onderzocht worden, hebben tot op heden een follow-up van ongeveer 6 jaar, en vanwege de lange tijd tussen het optreden van de HPV-infectie en het ontstaan van kanker is dit te kort om de effectiviteit tegen baarmoederhalskanker na te gaan. Bij dit gebrek aan informatie schat de Gezondheidsraad de uiteindelijke effectiviteit van het vaccin tegen baarmoederhalskanker op maximaal 54%. De raad gaat daarbij uit van een werkzaamheid tegen HPV16/18-infecties van 90%, een niet-selectieve opkomst voor de vaccinatie van 85% en het gegeven dat 70% van de gevallen van baarmoederhalskanker door HPV16/18 veroorzaakt wordt. 1 Vaccinatie met een van de 2 thans beschikbare vaccins, Gardasil, bleek na 6 jaar bij HPV16/18-negatieve vrouwen van 15-26 jaar voor 98% (95%-BI: 93-100) te beschermen tegen afwijkingen die gepaard gaan met een verhoogd risico op baarmoederhalskanker en die samengaan met HPV16/18, dat wil zeggen cervicale intra-epitheliale neoplasie (CIN) graad 2/3 en adenocarcinoma in situ. 6 Tegen alle afwijkingen ernstiger dan of gelijk aan CIN graad 1, dus ook tegen niet-HPV16/18-gerelateerde afwijkingen, werd de werkzaamheid geschat op 31% (95%-BI: 0-57). 7 Aangezien wij ervan uitgaan dat bijna alle 12-jarige meisjes HPV16/18-negatief zijn, zijn deze laatste gegevens het interessantst. Deze resultaten zijn echter afkomstig uit slechts één trial, die een follow-up van maar 4 jaar had; bovendien zijn ze onzeker door kleine onderzoeksaantallen. Omdat de werkzaamheid sterk afneemt in een populatie waar HPV16/18 aanwezig is, 6 zal vaccinatie van meisjes van 13-16 jaar, die voor een deel al seksueel actief zijn en daardoor misschien al geïnfecteerd (www.seksonderje25e.nl/resultaten_sept/index2.html), minder effectief zijn dan die van 12-jarigen.
Herhaalvaccinaties. De Gezondheidsraad geeft aan dat er op termijn één, maar mogelijk ook meer herhaalvaccinaties noodzakelijk kunnen zijn. 1 Bij de berekening van doelmatigheid in het geval van revaccinatie gaat de raad uit van slechts één herhaalvaccinatie op 30-jarige leeftijd; het scenario van meerdere herhaalvaccinaties wordt niet berekend. Omdat de noodzaak en de effecten hiervan in de beschikbare literatuur door de beperkte follow-up nog niet bekeken konden worden, zullen ook gevaccineerden in de toekomst deel moeten nemen aan het conventionele screeningsprogramma. Aangezien een kwart van de populatie met het huidige screeningsprogramma niet bereikt wordt, en het daarbij gaat om een hoogrisicogroep voor baarmoederhalskanker, 3 8 is de aanname van de Gezondheidsraad dat 100% van de vrouwen opkomt bij revaccinatie naar onze mening onrealistisch.
Typevervanging. Bij vaccinatie tegen de HPV-typen 16 en 18 kan een toename optreden van infecties met niet-vaccingerelateerde hoogrisico-HPV-typen (‘typevervanging’; ‘type replacement’), wat zou kunnen leiden tot een verminderde effectiviteit van het vaccin. Voor wat betreft de typevervanging merkt de Gezondheidsraad op dat deze potentiële problemen zich in de praktijk wellicht zullen manifesteren en beveelt daarvoor monitoring aan. 1
Effect op screening. Het is opmerkelijk dat de raad de eventuele aanpassing van de huidige screening op baarmoederhalskanker niet in het advies behandelt. Doordat vaccinatie de HPV16/18-positieve afwijkingen aan de baarmoederhals voorkómt, is het risico dat een met screening gevonden niet-invasieve afwijking uiteindelijk kanker wordt, verkleind – de prevalentie van HPV16/18 is namelijk groter naarmate de ernst van de afwijking groter is. 9 Dit betekent dat relatief meer vrouwen onnodig behandeld zullen worden voor een dergelijke afwijking, die bij screening is ontdekt. Bovendien moet rekening gehouden worden met een verminderde opkomst voor het bevolkingsonderzoek, omdat gevaccineerde vrouwen zouden kunnen denken voldoende beschermd te zijn.
doen bijwerkingen van de vaccinatie afbreuk aan de positieve gezondheidseffecten?
In het advies wordt onzes inziens het huidige gebrek aan data over veiligheid van de vaccins onvoldoende serieus genomen. Zo schrijft de raad dat de bijwerkingen op lange termijn inderdaad onbekend zijn, maar dat het gebruik van steeds zuiverder vaccins bij subgroepen tot immunologische bijwerkingen zou kunnen leiden. In de trial met Gardasil hadden gevaccineerde vrouwen 2,5 keer zo vaak klachten die zouden kunnen wijzen op immunologisch gemedieerde aandoeningen als vrouwen die een placebo hadden ontvangen. 1 Vanwege de kleine aantallen is deze factor echter onzeker en kan in een grotere populatie groter dan wel kleiner blijken te zijn. De raad meent dat op deze potentiële problemen in de praktijk moet worden gelet via monitoring na invoering van de vaccinatie. Dit laatste verbaast ons temeer omdat het voorstel is om meisjes van 12 jaar te gaan vaccineren, terwijl er in de trials over deze leeftijdsgroep nauwelijks gegevens zijn. Het is niet uitgesloten dat een grotendeels premenarchale groep anders zou kunnen reageren dan de onderzoekspopulatie van 15-26-jarigen. Onderzoek in een grote groep 12-jarigen is daarom aangewezen om de veiligheid van vaccinatie in de doelgroep vast te stellen, alvorens een vaccinatieprogramma voor de totale populatie kan worden gestart.
Een bijkomend voordeel van uitstel van vaccinatie is dat er intussen langduriger follow-upgegevens beschikbaar komen van personen in de reeds gevaccineerde populaties in andere landen. Daarbij moet worden opgemerkt dat zelfs zeldzame ernstige bijwerkingen van het vaccin consequenties kunnen hebben voor de verhouding tussen risico’s en baten, aangezien baarmoederhalskanker ook een zeldzame aandoening is.
is de kosten-effectiviteitverhouding gunstig ten opzichte van andere mogelijkheden van preventie?
De kosten-effectiviteitsverhouding van HPV-vaccinatie ligt boven de drempelwaarde van kosteneffectiviteit en is veel minder gunstig dan bijvoorbeeld de kosten-effectiviteitsverhouding van screening op baarmoederhalskanker. 1 Minister Klink geeft in zijn brief aan de Tweede Kamer aan dat het uitgangspunt voor uiteindelijke toevoeging van het vaccin aan het Rijksvaccinatieprogramma is dat de vaccinatie kosteneffectief moet kunnen worden uitgevoerd (www.minvws.nl/kamerstukken/pg/2008/vaccinatie-tegen-baarmoederhalskanker.asp). Echter, iedere berekening van de kosteneffectiviteit van HPV-vaccinatie berust op aannamen, omdat de effectiviteit niet bekend is. Zelfs onder zeer gunstige assumpties, namelijk dat het vaccin levenslang zou beschermen en dat er geen typevervanging optreedt, is de kosten-effectiviteitsratio voor vaccinatie hoger dan de in Nederland gehanteerde drempelwaarde van kosteneffectiviteit van € 20.000,– per gewonnen voor kwaliteit gecorrigeerd levensjaar (QALY); die varieert namelijk, afhankelijk van het model, van € 21.000,– tot € 30.000,– per gewonnen QALY. 1 De schatting van de kosten-effectiviteitverhouding van het huidige screeningsprogramma, die varieert van € 600,– tot € 3400,– per gewonnen QALY, is vele malen gunstiger dan die van vaccinatie. 1 Indien te zijner tijd herhaalvaccinaties nodig blijken te zijn, komen de kosten per gewonnen QALY nog hoger te liggen. De Gezondheidsraad onderkent dit, maar geeft desondanks een positief advies.
discussie over de prioriteit
Gezien de bovengenoemde argumenten vinden wij invoering van HPV-vaccinatie in het Rijksvaccinatieprogramma per 1 september 2009 onwenselijk. De snelheid waarmee deze invoering wordt voorgesteld staat in schril contrast met de zorgvuldige introductie van andere landelijke preventieprogramma’s, zoals het bevolkingsonderzoek op dikkedarmkanker, terwijl dikkedarmkanker toch een aandoening is waaraan jaarlijks 4500 mensen sterven en waarvoor een weinig belastende screeningstest bestaat, die het bevolkingsonderzoek waarschijnlijk zelfs kosteneffectiever maakt dan de screening op borst- of baarmoederhalskanker. Nadat de effectiviteit in sterftereductie van dit bevolkingsonderzoek op dikkedarmkanker al in de jaren negentig van de vorige eeuw was aangetoond, werd voor een Nederlands screeningsprogramma gepleit in 2002 en in 2004, en lopen er sinds 2006 3 proefbevolkingsonderzoeken in de regio’s Amsterdam, Nijmegen en Rotterdam. Er worden geen landelijke besluiten genomen vóór de resultaten uit deze trials bekend zijn. 10
Finland is sterk vergelijkbaar met Nederland wat betreft de zorgvuldige besluitvorming over preventie van kanker. In Finland vindt men het nog te vroeg om nu reeds een landelijke HPV-vaccinatie in te voeren. Een werkgroep van het National Public Health Institute in Helsinki voert de komende jaren een gerandomiseerd onderzoek uit bij 60.000 schoolkinderen (jongens en meisjes van 14 à 15 jaar oud); de eerste resultaten van deze trial worden in 2012-2014 verwacht (www.ktl.fi/portal/suomi/osastot/roko/ajankohtaista).
Ook in Nederland vindt doorgaans het opnemen van een vaccinatie in het Rijksvaccinatieprogramma niet lichtvaardig plaats. Zo stelt de Gezondheidsraad dat vóór invoering geheel of gedeeltelijk aan 7 criteria moet worden voldaan. 1 Zoals wij hebben aangegeven, zijn wij van mening dat landelijke invoering van een HPV-vaccinatie per 1 september 2009 te vroeg is, omdat aan 5 van deze 7 criteria van de Gezondheidsraad nog niet of niet volledig wordt voldaan.
Ons inziens heeft de Nederlandse vrouwelijke bevolking geen baat bij haastige invoering van HPV-vaccinatie, maar bij een goed opgezet onderzoek onder 12-jarigen, waarbij men aan alle aspecten van vaccinatie zoals hierboven beschreven aandacht zal moeten besteden. Bovendien zal in de loop van de komende jaren meer kennis worden verkregen over effectiviteit en neveneffecten door langere follow-up in de lopende trials. Dan zal een beter antwoord op veel van bovenstaande vragen gegeven kunnen worden en kan gedegen besluitvorming plaatsvinden over invoering en organisatie van HPV-vaccinatie.
Belangenconflict: geen gemeld. Financiële ondersteuning: prof.dr.J.D.F.Habbema en mw.drs.I.M.C.M.de Kok nemen binnen hun aanstelling aan het Erasmus MC deel aan onafhankelijk wetenschappelijk contractonderzoek met GlaxoSmithKline.
Aanvaard op 18 augustus 2008
Erasmus MC, afd. Maatschappelijke Gezondheidszorg, Postbus 2040, 3000 CA Rotterdam. Mw.drs.I.M.C.M.de Kok en hr.prof.dr.J.D.F.Habbema, epidemiologen; hr.prof.dr.J.W.W.Coebergh, sociaal-geneeskundige en epidemioloog (tevens: Integraal Kankercentrum Zuid, sectie Onderzoek, Eindhoven). Universitair Medisch Centrum Groningen, afd. Gynaecologie, Groningen. Mw.prof.dr.M.J.E.Mourits, gynaecologisch oncoloog. Nederlands Kanker Instituut, afd. Epidemiologie, Amsterdam. Mw.prof.dr.ir.F.E.van Leeuwen, epidemioloog. Correspondentieadres: mw.drs.I.M.C.M.de Kok (i.dekok@erasmusmc.nl).
Literatuur
1 Vaccinatie tegen baarmoederhalskanker. Den Haag: Gezondheidsraad; 2008.
2 Rossum TGJ van, Melker HE de, Houweling H, Voordouw ACG, Meijer CJLM, Helmerhorst ThJM, et al. Vaccins tegen Humaan papillomavirus (HPV); tussen registratie en implementatie. Ned Tijdschr Geneeskd. 2008;152:987-92.
3 Rebolj M, Ballegooijen M van, Berkers LM, Habbema D. Monitoring a national cancer prevention program: successful changes in cervical cancer screening in the Netherlands. Int J Cancer. 2007;120:806-12.
4 Aa MA van der, Pukkala E, Coebergh JW, Anttila A, Siesling S. Mass screening programmes and trends in cervical cancer in Finland and the Netherlands. Int J Cancer. 2008;122:1854-8.
5 Aa MA van der, Schutter EM, Looijen-Salamon M, Martens JE, Siesling S. Differences in screening history, tumour characteristics and survival between women with screen-detected versus not screen-detected cervical cancer in the east of the Netherlands, 1992-2001. Eur J Obstet Gynecol Reprod Biol. 2008;139:204-9.
6 Ault KA. Effect of prophylactic human papillomavirus L1 virus-like-particle vaccine on risk of cervical intraepithelial neoplasia grade 2, grade 3, and adenocarcinoma in situ: a combined analysis of four randomised clinical trials. Lancet. 2007;369:1861-8.
7 Mao C, Koutsky LA, Ault KA, Wheeler CM, Brown DR, Wiley DJ, et al. Efficacy of human papillomavirus-16 vaccine to prevent cervical intraepithelial neoplasia: a randomized controlled trial. Obstet Gynecol. 2006;107:18-27.
8 Oortmarssen GJ van, Habbema JD. Epidemiological evidence for age-dependent regression of pre-invasive cervical cancer. Br J Cancer. 1991;64:559-65.
9 Clifford G, Franceschi S, Diaz M, Muńoz N, Villa LL. Chapter 3: HPV type-distribution in women with and without cervical neoplastic diseases. Vaccine. 2006;24 Suppl 3:S26-34.
10 Signaleringscommissie Kanker van KWF Kankerbestrijding. Vroege opsporing van dikkedarmkanker. Amsterdam: Nederlandse Kankerbestrijding/Koningin Wilhelmina Fonds; 2004.
HPV-vaccinatie weinig zinvol
Publicatie: 21 november 2008
Auteur: L.J. Boomsma, A.J.M. Drenthen en C.J. in ’t Veld
Meer aandacht voor risicofactoren baarmoederhalskanker
De auteurs zijn betrokken bij het project ‘Preventie: maatwerk’ van de LVG/NHG dat onder meer de uitvoering van het bevolkingsonderzoek baarmoederhalskanker in de huisartsenpraktijk als aandachtspunt heeft.
De combinatie van het bevolkingsonderzoek naar baarmoederhalskanker en vaccinatie van meisjes tegen het humaanpapillomavirus kost veel geld en levert betrekkelijk weinig op. De overheid kan het geld beter steken in onderzoek naar risicofactoren van de ziekte.
De Gezondheidsraad heeft de minister van VWS geadviseerd om vaccinatie tegen het humaanpapillomavirus (HPV) in te voeren voor meisjes. De raad denkt dat zo de morbiditeit en mortaliteit door baarmoederhalskanker kan worden gehalveerd, al ontbreekt daarvoor nog het bewijs.1 Er klinken ook andere geluiden.
Zo zou HPV-vaccinatie onvoldoende werkzaam zijn, zou er mogelijk sprake zijn van (ernstige) bijwerkingen als tot anafylaxie kunnen leiden en is vaccinatie niet erg kosteneffectief.2 3 Maar volgens de Gezondheidsraad heeft het onderzoek waarop deze argumenten zijn gebaseerd geen nieuwe gezichtspunten opgeleverd en dus ziet de raad geen reden om het advies aan de minister te herzien.4
Bij vaccinatie tegen HPV spelen drie problemen. Het eerste is een gebrek aan individualisatie. Veel onderzoeken zijn gebaseerd op grote aantallen patiënten die een interventie krijgen, terwijl de terugkoppeling naar het individu moeilijk is te maken. Een ander probleem is het beperkte inzicht in de pathofysiologie van het virus. Het derde probleem is de marketing: door de ontwikkeling van bepaalde medicijnen ontstaat door lobby opeens ook een vraag en een doelgroep.
Grote getallen
Bij preventie gaat het om het number needed to screen (NNS) en het number needed to vaccinate (NNV), ofwel het aantal personen dat onderzocht respectievelijk gevaccineerd moet worden om één sterfgeval door de aandoening te voorkomen. Het NNS is te berekenen aan de hand van de sterfte en de absolute risicoreductie van het preventieprogramma. Daarbij geldt NNS=1/absolute risicoreductie. Deze waarden zijn voor de meeste preventieprogramma’s bekend.5
Het NNS voor het bevolkingsonderzoek op baarmoederhalskanker is 2560 uitstrijkjes (3600 oproepen bij een deelname van 70%) om per jaar één sterfgeval aan baarmoederhalskanker te voorkomen (zie tabel 1). Dezelfde berekening voor HPV-vaccinatie levert een NNV op van 100.000, ongeveer de grootte van een leeftijdscohort. Bij een opkomstpercentage van 85% moeten jaarlijks 85.000 vaccinaties worden uitgevoerd om minder dan één sterfgeval te voorkomen (zie tabel 2). In combinatie met het bevolkingsonderzoek wordt het NNV dubbel zo groot.
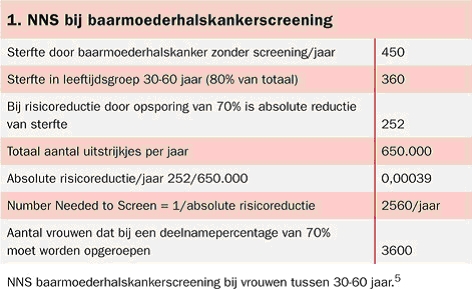
Dat geldt ook voor het NNS: er zijn 5100 uitstrijkjes (7200 oproepen) nodig om één sterfgeval te voorkomen (zie tabel 3). Dat betekent dat de geplande opzet van het bevolkingsonderzoek baarmoederhalskanker aangevuld met HPV-vaccinatie een enorme inspanning van de gezondheidszorg vraagt. Er moeten grote aantallen meisjes (226.000) voor vaccinatie en twee keer zoveel vrouwen (7200) als in de huidige situatie worden uitgenodigd voor het bevolkingsonderzoek, met een zeer beperkte winst als we uitgaan van sterfte.
Schadelijke virussen
Het tweede probleem is het beperkte inzicht in de pathofysiologie van HPV. Van het virus zijn verschillende typen bekend waarvan er een aantal schadelijk is. De meeste vrouwen raken door seks besmet met HPV, maar het lichaam ruimt het virus vaak ook weer op. Onduidelijk is welke vrouwen het virus niet opruimen.
Heeft dit te maken met het virusaanbod door bijvoorbeeld wisselende contacten of met de weerstand van de vrouw? Zijn er kenmerken die meer inzicht geven in een groter risico op het persisteren van HPV? Denk bijvoorbeeld aan een vroege sexarche, wisselende contacten, soa’s, regelmatig fluor vaginalis, roken en HPV-gerelateerde infecties als wratten, mollusca, dermatofibromen en condylomen.

Bekend is dat de cellulaire immuniteit die HPV moet klaren afneemt onder invloed van oestrogene hormonen. Daardoor persisteert HPV bij gebruik van orale anticonceptiva langer en daarmee neemt het risico op premaligne afwijkingen van de cervix toe. Dit risico wordt echter weer gecompenseerd door een afname van de incidentie van andere gynaecologische carcinomen.6
Een beslisregel zoals bij het inschatten van het cardiovasculaire risico en bij het risico op diepe veneuze trombose zou vrouwen kunnen identificeren die een groter risico lopen op baarmoederhalskanker.7 8 Deze vrouwen zouden dan in aanmerking komen voor een uitstrijkje en HPV-diagnostiek. Inmiddels is wel bekend dat HPV-vaccinatie antistoffen oproept en dat vrouwen met persisterende HPV-infecties lage antistoftiters hebben.
Dat doet vermoeden dat het mogelijk is om bij aanwezigheid van HPV het immuunsysteem te activeren met een vaccinatie(serie), die het virus vernietigt. De vaccinatie kan dan zowel preventief (geïndiceerde preventie) worden ingezet bij vrouwen die HPV dragen zonder portioafwijkingen, als bij premaligne afwijkingen, zoals intra-epitheliale neoplasie. Als het virus dieper doordringt in de cervix, zal het immuunsysteem van de vrouw worden geactiveerd en is van vaccinatie weinig meer te verwachten.
Denk ook aan de partner van de vrouw. Een man met persisterende HPV infecteert steeds zijn echtgenote en heeft ook zelf een risico op maligniteiten in de anogenitale regio. Het zou niet verwonderlijk zijn als HPV behalve bij penis- en anuscarcinoom ook een rol speelt bij prostaatcarcinoom. Er is kortom meer inzicht nodig in de relatie tussen gastvrouw (en gastheer) en het persisteren van HPV om risicogroepen te identificeren en een beslisregel te ontwikkelen.

Onafhankelijkheid
Deskundigen worden uitgenodigd plaats te nemen in commissies, voordrachten
te houden en onderzoeksaanvragen te beoordelen. Als opinieleiders vormen
zij een belangrijke, invloedrijke doelgroep van de farmaceutische
industrie. Gezien de belangrijke derde geldstroom in het wetenschappelijk
onderzoek is het als onderzoeker moeilijk de geclaimde onafhankelijkheid
vol te houden.
Daarnaast dreigt de invoering van HPV-vaccinatie een politieke keuze te
worden die wordt gestuurd door angst voor actiegroepen of stemmenverlies.
Nederland wil niet achterblijven als de rest van Europa wel overgaat tot
vaccinatie tegen HPV. De politiek moet beseffen dat het
bevolkingsonderzoek baarmoederhalskanker in andere landen minder goed is
georganiseerd. De sterftecijfers voor baarmoederhalskanker zijn in
Nederland zeer gunstig bij een relatief lang screeningsinterval van 5
jaar.9
Scenario’s
Nederland heeft een aantal mogelijkheden. In de eerste optie blijft het
huidige bevolkingsonderzoek gehandhaafd. Bij vrouwen met laaggradige
afwijkingen aan de cervix volgt een HPV-bepaling. Bij een positieve
uitslag wordt onderzocht of een vaccinatieschema effectief kan zijn.
Verder handelen artsen volgens de bestaande richtlijnen. Voor vrouwen die
moeilijk te bereiken zijn met het bevolkingsonderzoek is het te overwegen
onderzoek op aanwezigheid van HPV in te voeren. Vrouwen uit deze groepen
komen eventueel ook in aanmerking voor HPV-vaccinatie.
In de tweede optie wordt naast het bevolkingsonderzoek
baarmoederhalskanker HPV-vaccinatie ingevoerd. Grote aantallen meisjes en
vrouwen worden opgeroepen. Het is te verwachten dat vanwege de vaccinatie
de bereidheid afneemt om een uitstrijkje te laten maken. Het oproepen en
herinneren van vrouwen voor het bevolkingsonderzoek kost veel tijd,
huisartsen haken af en de beschermingsgraad daalt nog verder. Andere
HPV-typen gaan prevaleren boven HPV 16/18. De incidentie van
baarmoederhalskanker neemt toe en vanwege het opheffen van de bestaande
structuur wordt Nederland hekkensluiter in Europa op het gebied van
baarmoederhalskanker (vergelijk ook de gang van zaken rond perinatale
sterfte).
Nederland kan er ook voor kiezen algemene HPV-vaccinatie niet in te
voeren: optie drie. Met het uitgespaarde geld wordt een onafhankelijk
(cohort)onderzoek uitgevoerd naar risicofactoren voor
baarmoederhalskanker. Dat levert een beslisschema op waarmee voor vrouwen
een risicoscore is te berekenen:
- Als de risicoscore baarmoederhalskanker vrijwel uitsluit, krijgt de
vrouw voorlichting. Verdere actie is niet nodig.
- Als de risicoscore baarmoederhalskanker niet uitsluit en op een
laag risico duidt, komt de vrouw in aanmerking voor een uitstrijkje al dan
niet aangevuld met HPV-screening. HPV-vaccinatie speelt mogelijk een rol
bij laaggradige cervixafwijkingen en aanwezig HPV, dat blijkbaar
onvoldoende immuunrespons oproept.
- Als de risicoscore een hoog risico op baarmoederhalskanker
aangeeft, komt de vrouw in aanmerking voor een uitstrijkje en
HPV-screening en regelmatige controles. HPV-vaccinatie kan een
mogelijkheid zijn, ook zonder cervixafwijkingen of positieve HPV-screening.
Hielprik
Het schot hagel op baarmoederhalskanker wordt met deze optie ingeruild
voor schieten met scherp. Dat biedt aanzienlijke voordelen: minder
slachtoffers, lagere kosten en meer effectiviteit.
Mogelijk kunnen DNA-technieken in de toekomst de vatbaarheid voor bepaalde
aandoeningen aangeven. Het DNA-profiel wordt na de geboorte middels de
hielprik in kaart gebracht. Bepaalde HLA-typen zouden mogelijk een
verhoogd risico geven op baarmoederhalskanker. Deze vrouwen worden
vervolgens hun leven lang gecontroleerd. Wel is het zo dat iedereen een
aantal potentieel schadelijke genen met zich meedraagt die maar zelden tot
expressie komen. De meeste aandoeningen zijn op meerdere genen
gelokaliseerd. Naast het genetisch materiaal is de omgeving van groot
belang bij het krijgen en het beloop van een ziekte. Genetische typering
lijkt voorlopig een weinig zinvolle optie.
Louwrens Boomsma, huisarts, wetenschappelijk medewerker NHG
dr. Ton Drenthen, senior wetenschappelijk medewerker NHG
Kees in ’t Veld, huisarts, hoofd afdeling Implementatie NHG
Correspondentieadres: l.boomsma@nhg.org
Referenties:
1. Gezondheidsraad. Vaccinatie tegen baarmoederhalskanker. Den Haag:
Gezondheidsraad, 2008; publicatienummer 2008/08 of via www.gr.nl.
2. Anonymus. Vaak allergische reactie na HPV-vaccin. Medisch Contact 2008;
63: 1461 (betreft CMAJ early online 1 sept 2008).
3. Kok IMCM de, Habbema JDF, Mourits MJE, Coebergh JWW, Leeuwen FE van,
Onvoldoende gronden voor opname van vaccinatie tegen Humaan papillomavirus
in het Rijksvaccinatieprogramma. Ned Tijdschr Geneeskd 2008; 152: 2001-4.
4. Reactie Gezondheidsraad op referentie 3 via www.gr.nl geraadpleegd 5
september 2008.
5. Boomsma LJ, Lidt de Jeude CP van. ‘Number Needed to Screen’; een
hulpmiddel bij de beoordeling van preventieprogramma’s. Ned Tijdschr
Geneeskd 2000; 144: 2345-8.
6. Appleby P, Beral V,
Berrington de GA, Colin D, Franceschi S, Goodhill A, et al. Cervical
cancer and hormonal contraceptives: collaborative reanalysis of individual
data for 16,573 women with cervical cancer and 35,509 women without
cervical cancer from 24 epidemiological studies. Lancet 2007; 70
(9599): 1609-1621.
7. NHG-Standaard Cardiovasculair Risicomanagement via www.nhg.org.
8. NHG-Standaard Diepe veneuze trombose via www.nhg.org.
9. Boomsma LJ, Assendelft WJJ. De Belgische Aanbeveling
cervixkanker-screening en de NHG-Standaard Cervixuitstrijken vergeleken.
Huisarts Wet 2003; 46: 205-6.